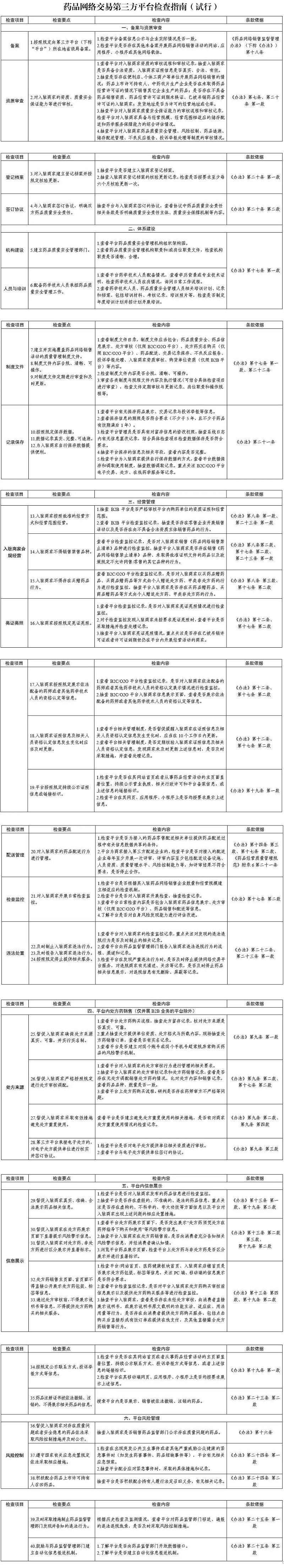
1月5日,国家药监局综合司发布通知,印发《药品网络交易第三方平台检查指南(试行)》(以下简称《检查指南》)。通知明确了常规检查重点考虑因素3项、有因检查重点考虑因素7项以及检查方式、检查地点等事项。《检查指南》列出40项检查要点以及其对应的检查内容。
根据通知内容
对药品网络交易第三方平台(以下简称第三方平台),常规检查重点考虑因素包括:首次开展第三方平台业务的;开展第三方平台业务无药品流通专业背景的;第三方平台经营规模大、覆盖范围广、业务量较大的。有因检查重点考虑因素包括:网络监测、群众信访、投诉举报、舆情信息、网络抽检等提示可能存在风险的;未能及时识别、发现、制止、报告相关风险的;未严格审核管理平台内药品信息、链接和药品销售活动的;既往多次检查不符合要求的;管理体系与关键岗位负责人发生重大调整的;未及时整改监督检查发现缺陷项的;药品监管部门认为需要开展检查的其他情况。
《检查指南》内容涵盖备案与资质审查、体系建设、经营管理、平台内处方药销售(仅开展B2B业务的平台除外)、平台内信息展示、平台风险管理六个方面,列出40项检查要点以及其对应的检查内容。例如,平台内处方药销售方面,督促入驻商家采取有效措施避免处方重复使用,要查看平台是否建立避免处方重复使用的相关措施,是否有对商家处方重复使用情况的检查记录。
国家药监局综合司关于印发药品网络交易第三方平台检查指南(试行)的通知
药监综药管函〔2023〕691号
各省、自治区、直辖市和新疆生产建设兵团药品监督管理局:
为指导药品监督管理部门开展药品网络交易第三方平台(以下简称第三方平台)检查工作,督促企业履行法定义务,落实平台主体责任,根据《药品网络销售监督管理办法》,国家药监局组织制定了《药品网络交易第三方平台检查指南(试行)》(以下简称检查指南),现予印发,请遵照执行。
检查指南适用于指导药品监督管理部门对提供第三方平台服务的企业开展监督检查工作。有关检查组织实施、检查机构和人员、检查程序、常规检查、有因检查、检查与稽查的衔接、跨区域检查协作、检查结果的处理等工作,按照《药品检查管理办法(试行)》等有关要求执行。
一、常规检查重点考虑因素
(一)首次开展第三方平台业务的;
(二)开展第三方平台业务无药品流通专业背景的;
(三)第三方平台经营规模大、覆盖范围广、业务量较大的。
二、有因检查重点考虑因素
(一)网络监测、群众信访、投诉举报、舆情信息、网络抽检等提示可能存在风险的;
(二)未能及时识别、发现、制止、报告相关风险的;
(三)未严格审核管理平台内药品信息、链接和药品销售活动的;
(四)既往多次检查不符合要求的;
(五)管理体系与关键岗位负责人发生重大调整的;
(六)未及时整改监督检查发现缺陷项的;
(七)药品监管部门认为需要开展检查的其他情况。
三、检查方式
检查方式包括现场检查和非现场检查。现场检查指检查人员到企业开展第三方平台业务的经营场所进行检查。非现场检查指采用网络巡查、网络监测、视频电话等方式开展检查。
检查组可根据工作需要采取现场检查和/或非现场检查方式。鼓励各地探索“线上线下相结合”“交叉互查”等检查方式,运用“以网管网”的技术工具丰富检查手段。
四、检查地点
检查地点主要为企业开展第三方平台业务的注册地址及其经营场所,必要时可对相关场所进行延伸检查。
五、其他事项
第三方平台药品质量安全管理机构负责人和具有系统后台操作权限的信息技术人员应当实地配合开展检查工作。检查人员参照检查指南的检查项目和所对应的重点检查内容开展检查。检查结束后,填写《药品网络交易第三方平台检查表(参考)》(附件),对不符合项目进行详细描述,并由检查组成员和企业进行现场确认。
检查发现企业违反《药品网络销售监督管理办法》等有关规定的,应当依法依规处置。
附件:药品网络交易第三方平台检查表(参考)
国家药监局综合司
2023年12月29日
声 明:转载此文是出于传递更多信息之目的。若有来源标注错误或侵犯了您的合法权益,请作者持权属证明与本网联系,我们将及时更正、删除,谢谢。联系电话:028-64775583,邮箱:kefu@zyctd.com。
为进一步落实《中共中央国务院关于促进中医药传承创新发展的意见》《国家药品监督管理局关于促进中药传承创新发展的实施意见》等对于鼓励中药二次开发、促进中药产业高质量发展的要求,指导申请人开展中药改良...
导读:国家药监局、国家中医药局组织制定了《地区性民间习用药材管理办法》,并于近日发布,自2024年11月1日起施行。地区性民间习用药材管理办法第一章总则第一条为加强地区性民间习用药材管理,满足临...
在4月22日上午举行的最高人民法院新闻发布会上,最高人民法院知识产权法庭副庭长郃中林表示,医药领域的科研成果直接关涉人民群众生命健康,医药领域也是技术创新难度和市场集中度相对较高的领域,既需要保...
中新网4月30日电据国家市场监督管理总局网站消息,4月30日,市场监管总局发布《保健食品原料人参西洋参灵芝备案产品技术要求》(以下简称《产品技术要求》),对以人参、西洋参、灵芝为原料的保健食品实...
【制药网政策法规】为促进按古代经典名方目录管理的中药复方制剂(以下简称中药3.1类)的研发和注册,4月25日,国家药监局药品审评中心发布施行《按古代经典名方目录管理的中药复方制剂药学申报资料撰写...